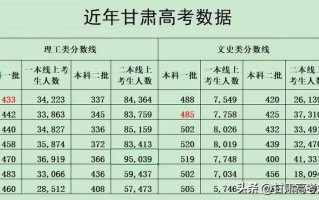
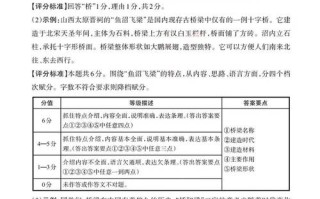
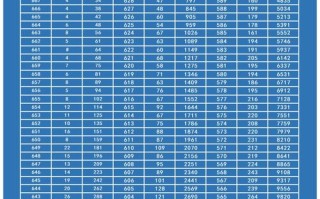
这次考试是山东省在2025年高考改革前使用“3+X”模式时,各地市组织的重要诊断性考试,其命题风格、题型设置和考点分布,都高度模拟了当年的全国新课标卷(山东是新课标卷的试点省份之一),对高三学生有极强的指导意义。
试卷整体分析
命题特点
- 紧扣考纲,注重基础:试卷全面覆盖了《考试说明》中的核心考点,如化学用语、阿伏伽德罗常数、元素周期律、化学反应原理、化学实验基础等,强调对基本概念和基本理论的考查。
- 突出主干,能力立意:重点考查了化学平衡、电解质溶液、电化学、有机化学合成与推断等主干知识,注重对学生信息获取、分析推理、实验设计和综合应用能力的考查。
- 联系实际,学以致用:部分题目背景来源于生活实际和工业生产(如海水提镁、燃料电池、药物合成等),体现了化学学科的实用价值。
- 题型稳定,结构清晰:全卷分为第I卷(选择题)和第II卷(非选择题),结构非常稳定,与高考模式完全一致。
考点分布
-
选择题(7题,42分):
- 化学与生活/STSE(第1题):考查基本化学常识。
- 阿伏伽德罗常数(第2题):经典考点,涉及气体摩尔体积、物质结构、氧化还原反应等。
- 离子方程式正误判断(第3题):高频考点,考查反应条件、物质拆分、电荷守恒等。
- 元素周期律与元素周期表(第4题):比较原子半径、金属性/非金属性、氢化物稳定性等。
- 有机化学基础(第5题):同分异构体、官能团性质、反应类型判断。
- 电化学(第6题):新型电池,考查正负极、电极反应式书写。
- 化学平衡与反应速率(第7题):图像分析,考查外界条件对平衡的影响。
-
非选择题(4大题,58分):
- 第26题 - 无机化工流程题:以“海水提镁”为背景,考查物质的分离提纯、离子方程式书写、物质转化、实验操作评价等。
- 第27题 - 化学原理综合题:包含两个小部分。
- (1) 化学反应速率与化学平衡:结合图像进行计算和平衡移动分析。
- (2) 电解质溶液:结合弱电解质电离和盐类水解,进行离子浓度大小比较和pH计算。
- 第28题 - 实验探究题:以“探究某盐的成分”为背景,考查实验设计、现象分析、结论评价等综合实验能力。
- 第29题 - 有机化学推断与合成题:以药物中间体的合成为背景,考查官能团衍变、反应类型判断、同分异构体书写、合成路线设计等。
重点试题解析与考点回顾
以下是对部分典型题目的解析,可以帮助你理解当时考查的重点和难点。
【选择题示例】
例1(第2题,阿伏伽德罗常数):
设NA为阿伏伽德罗常数的值,下列说法正确的是 A. 1 mol/L NaCl溶液中含有NA个Na⁺ B. 1 mol Fe与足量稀硝酸反应,转移的电子数为2NA C. 标准状况下,22.4 L HF中含有分子数为NA D. 1 mol Na2O2与足量CO2反应,转移的电子数为NA
解析:
- A. 错误,缺少溶液的体积,无法计算Na⁺的物质的量。
- B. 错误,Fe与稀硝酸反应生成Fe³⁺,化学方程式为:Fe + 4HNO₃(稀) = Fe(NO₃)₃ + NO↑ + 2H₂O,1 mol Fe失去3 mol电子,转移电子数为3NA。
- C. 错误,标准状况下,HF是液体,不能使用气体摩尔体积22.4 L/mol进行计算。
- D. 正确,反应为:2Na₂O₂ + 2CO₂ = 2Na₂CO₃ + O₂,Na₂O₂中氧元素化合价由-1价变为0价和-2价,属于歧化反应,1 mol Na₂O₂参与反应时,有1 mol O⁻被氧化为O₂(失去1 mol电子),同时有1 mol O⁻被还原为Na₂CO₃(得到1 mol电子),所以转移电子数为NA。
考点回顾:阿伏伽德罗常数是每年必考的“送分”或“送命题”,需要特别注意:① 物质的状态和体积;② 物质的聚集状态(如HF、H₂O在标况下为液态);③ 溶液中溶质的浓度与离子数的关系(需知体积);④ 氧化还原反应中电子转移的数目(看清化合价变化和物质的量关系)。
【非选择题示例】
例2(第27题,化学原理综合):
(1) 在2 L密闭容器中,充入2 mol A和1 mol B,在一定条件下发生反应:2A(g) + B(g) ⇌ xC(g),2 min后达到平衡,测得A的浓度为0.6 mol/L,C的体积分数为0.25,则: ① x = ______; ② 0~2 min内,B的平均反应速率为 ______; ③ 该反应的平衡常数K = ______。
(2) 常温下,将amol/L的氨水与bmol/L的盐酸等体积混合,反应后溶液呈中性(忽略混合后体积变化),则: ① a与b的大小关系为a ______ b(填“>”、“<”或“=”); ② 用a、b表示该混合液中NH₄⁺的浓度为 ______ mol/L。
解析:
-
(1) 化学平衡计算
- ① 求x:
- 初始浓度:c(A) = 1 mol/L, c(B) = 0.5 mol/L
- 变化浓度:Δc(A) = 1 - 0.6 = 0.4 mol/L
- 根据方程式系数比,Δc(B) = 0.4 / 2 = 0.2 mol/L
- Δc(C) = 0.4 * (x/2) = 0.2x mol/L
- 平衡时,c(C) = 0.2x mol/L
- 根据C的体积分数:c(C) / [c(A) + c(B) + c(C)] = 0.25
- 代入数据:0.2x / (0.6 + 0.3 + 0.2x) = 0.25
- 解得:x = 2
- ② 求v(B):
v(B) = Δc(B) / t = 0.2 mol/L / 2 min = 0.1 mol/(L·min)
- ③ 求K:
- 平衡浓度:c(A) = 0.6 mol/L, c(B) = 0.5 - 0.2 = 0.3 mol/L, c(C) = 0.2 * 2 = 0.4 mol/L
- K = c²(C) / [c²(A) c(B)] = (0.4)² / [(0.6)² 0.3] = 16 / 54 = 8 / 27
- ① 求x:
-
(2) 电解质溶液
- ① a与b的关系:
- 氨水与盐酸反应:NH₃·H₂O + HCl = NH₄Cl + H₂O
- 反应后溶液呈中性,说明NH₄⁺水解产生的H⁺与NH₃·H₂O电离产生的OH⁻恰好抵消,NH₄⁺水解是微弱的,所以溶液中剩余的NH₃·H₂O的浓度必须大于NH₄⁺的浓度,才能保证中性。
- 反应前n(NH₃·H₂O) = aV, n(HCl) = bV,反应后,n(NH₃·H₂O) = (a-b)V, n(NH₄⁺) = bV。
- 因为溶液呈中性,c(NH₃·H₂O) > c(NH₄⁺),即 (a-b) > b,解得 a > 2b。
- (注:原题中“等体积混合”和“呈中性”是关键,更精确的解法是利用电荷守恒和质子守恒,在NH₄Cl和NH₃·H₂O的混合液中呈中性,必有 c(NH₄⁺) + c(H⁺) = c(Cl⁻) + c(OH⁻),因c(H⁺)=c(OH⁻),c(NH₄⁺) = c(Cl⁻),c(Cl⁻)由盐酸决定,为b/2 mol/L,c(NH₄⁺)由反应的盐酸决定,也为b/2 mol/L,而c(NH₃·H₂O)初始为a/2 mol/L,反应掉b/2 mol/L,剩余(a-b)/2 mol/L,因为溶液呈中性,NH₃·H₂O的电离程度大于NH₄⁺的水解程度,所以剩余的c(NH₃·H₂O) > c(NH₄⁺),即 (a-b)/2 > b/2,解得 a > 2b。)
- ② 求c(NH₄⁺):
- 反应后,NH₄⁺完全由盐酸反应生成,其物质的量等于盐酸的物质的量。
- n(NH₄⁺) = n(HCl) = bV
- 混合后总体积为2V
- c(NH₄⁺) = n(NH₄⁺) / 2V = bV / 2V = b/2 mol/L
- ① a与b的关系:
考点回顾:
- 化学平衡:三段式法是核心,必须熟练掌握,注意利用体积分数、转化率等数据建立方程求解未知数(如本题中的x),平衡常数K的表达式和计算是重中之重。
- 电解质溶液:比较离子浓度大小、判断溶液酸碱性是常考点,核心是掌握三大守恒(电荷守恒、物料守恒、质子守恒)和两大理论(弱电解质的电离平衡、盐类的水解平衡),本题中,判断a和b的关系是难点,需要理解“中性”的微观含义。
对当前备考的启示
虽然这是2025年的联考试题,但其考查的思路和能力要求在今天依然具有很高的参考价值。
- 回归基础,狠抓核心:无论高考如何改革,化学的基本概念、基本理论、基本实验都是不变的,像阿伏伽德罗常数、离子方程式、化学平衡、电化学、有机反应等主干知识,必须做到烂熟于心。
- 强化计算,规范书写:化学计算是理科思维的体现,要熟练掌握物质的量、反应速率、平衡常数、溶液pH等计算,化学用语(方程式、离子方程式、电极反应式)的书写必须规范,这是化学的“书面语”。
- 提升综合应用能力:流程题、实验探究题、有机推断题是区分度较高的题型,备考时要学会从题目中提取有效信息,将新知识与旧知识结合,建立解题模型,看到流程图就要想到“除杂、分离、提纯、转化”;看到实验就要想到“目的、原理、步骤、现象、误差分析”。
- 关注STSE,拓展视野:化学源于生活,用于社会,多关注与化学相关的科技前沿、环境问题、生产生活实际,培养化学学科素养。
希望这份详细的解析能帮助你更好地理解2025年日照联考化学的特点,并为你的化学学习提供有益的参考。
标签: 2025日照联考化学重点考点 2025日照联考化学备考指南 2025日照联考化学命题趋势